√Pembahasan Soal Hukum Gas ⊗ Full Pembahasanya
Pembahasan soal hukum gas
1. EBTANAS-SMP-02-06
Volume gas mula-mula 2 m3 , mempunyai tekanan 1 atmosfer. Supaya tekanannya menjadi 4 atmosfer pada suhu yang tetap, maka volume gas harus dijadikan …
A. 0,25 m3
B. 0,50 m3
C. 0,75 m3
D. 1,25 m3
Pembahasan
Diketahui :
Volume awal (V1) = 2 m3
Tekanan awal (P1) = 1 atmosfer
Tekanan akhir (P2) = 4 atmosfer
Ditanya : Volume akhir (V2)
Jawab :
Rumus hukum Boyle (proses isotermal atau suhu konstan) :
P1 V1 = P2 V2
(1 atm)(2 m3) = (4 atm)(V2)
2 m3 = 4 (V2)
V2 = (2/4) m3
V2 = 1/2 m3
V2 = 0,5 m3
Jawaban yang benar adalah B.
Ebook Soal UN Fisika SMP/MTs Tahun 2000 - 2014 dan Kunci Jawaban 1,4 MB Ebook pembahasan soal Ujian Nasional IPA fisika SMP/MTs tahun 2000-2014 565 kBPembahasan soal hukum gas
1. EBTANAS-SMP-02-06
Volume gas mula-mula 2 m3 , mempunyai tekanan 1 atmosfer. Supaya tekanannya menjadi 4 atmosfer pada suhu yang tetap, maka volume gas harus dijadikan …
A. 0,25 m3
B. 0,50 m3
C. 0,75 m3
D. 1,25 m3
Pembahasan
Diketahui :
Volume awal (V1) = 2 m3
Tekanan awal (P1) = 1 atmosfer
Tekanan akhir (P2) = 4 atmosfer
Ditanya : Volume akhir (V2)
Jawab :
Rumus hukum Boyle (proses isotermal atau suhu konstan) :
P1 V1 = P2 V2
(1 atm)(2 m3) = (4 atm)(V2)
2 m3 = 4 (V2)
V2 = (2/4) m3
V2 = 1/2 m3
V2 = 0,5 m3
Jawaban yang benar adalah B.
Ebook Soal UN Fisika SMP/MTs Tahun 2000 - 2014 dan Kunci Jawaban 1,4 MB Ebook pembahasan soal Ujian Nasional IPA fisika SMP/MTs tahun 2000-2014 565 kBPembahasan soal hukum gas ideal
1. Soal UN 2007/2008 P4 No.18
Sebanyak 3 liter gas Argon bersuhu 27°C pada tekanan 1 atm (1 atm = 105 Pa) berada di dalam tabung. Jika konstanta gas umum R = 8,314 J.mol−1.K−1 dan banyaknya partikel dalam 1 mol gas 6,02 x 1023 partikel, maka banyak partikel gas Argon dalam tabung tersebut adalah…..
A. 0,83 x 10 23 partikel
B. 0,72 x 10 23 partikel
C. 0,42 x 10 23 partikel
D. 0,22 x 10 23 partikel
E. 0,12 x 10 23 partikel
Pembahasan
Diketahui :
Volume gas = 3 liter = 3 dm3 = 3 x 10-3 m3
Suhu gas = 27oC + 273 = 300 K
Tekanan gas = 1 atm = 105 Pa
Konstanta gas umum (R) = 8,314 J.mol−1 .K−1
Bilangan Avogadro (NA) = 6,02 x 1023 molekul/mol
Ditanya : banyaknya partikel gas argon dalam tabung
Jawab :

2. Soal UN Fisika SMA/MA U-ZC-2013/2014 No.18
Suatu gas ideal berada dalam suatu bejana tertutup dengan tekanan P, volume V, dan suhu T. Jika suatu saat suhu diubah menjadi 2T, dan volumenya menjadi 3/2 V, maka perbandingan tekanan awal (P1) dengan tekanan akhir (P2) setelah V dan T diubah adalah….
A. 1 : 3
B. 1 : 2
C. 2 : 3
D. 3 : 4
E. 4 : 3
Pembahasan
Diketahui :
Tekanan awal (P1) = P
Volume awal (V1) = V
Volume akhir (V2) = 3/2 V
Suhu awal (T1) = T
Suhu akhir (T2) = 2T
Ditanya : Perbandingan tekanan awal (P1) dan tekanan akhir (P2)
Jawab :
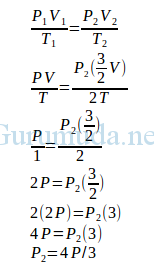
Perbandingan tekanan awal dan akhir :
P1 : P2
P : 4P/3
1 : 4/3
3 (1) : (3) 4/3
3 : 4
Jawaban yang benar adalah D.
3. Soal UN Fisika SMA/MA U-ZC-2013/2014 No.18
Gas oksigen dengan volume V, suhu T, dan tekanan P berada dalam silinder yang ditutup dengan klep. Bila klep ditekan, volume oksigen menjadi 3/4 V dan suhu menjadi 3/2 T, maka perbandingan tekanan awal dan tekanan akhir gas adalah….
A. P1 : P2 = 1 : 2
B. P1 : P2 = 2 : 3
C. P1 : P2 = 3 : 2
D. P1 : P2 = 3 : 4
E. P1 : P2 = 4 : 3
Pembahasan
Diketahui :
Tekanan awal (P1) = P
Volume awal (V1) = V
Volume akhir (V2) = 3/4 V
Suhu awal (T1) = T
Suhu akhir (T2) = 3/2 T
Ditanya : Perbandingan tekanan awal (P1) dan tekanan akhir (P2)
Jawab :
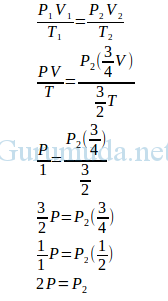
Perbandingan tekanan awal dan akhir :
P1 : P2
P : 2P
1 : 2
Jawaban yang benar adalah A.
Teori kinetik gas 91.15 KB

0 Response to "√Pembahasan Soal Hukum Gas ⊗ Full Pembahasanya"
Posting Komentar