√Pembahasan Soal Teori Kinetik Gas ⊗ Full Pembahasanya
Pembahasan soal teori kinetik gas
1. Soal UN 2007/2008 P4 No.19
Tekanan gas ideal di dalam ruang tertutup terhadap dinding tabung dirumuskan :
P = 2N/3V EK
P = tekanan (Pa)
N = jumlah molekul (partikel) gas
V = volume gas
EK = energi kinetik rata-rata molekul (J).
Pernyataan yang benar terkait rumusan di atas adalah…
A. Tekanan gas terhadap dinding tergantung pada jumlah molekul per satuan volume
B. Energi kinetik gas tidak tergantung pada tekanan yang ditimbulkan molekul terhadap dinding
C. Volume gas dalam tabung tidak berubah jika tekanan gas berubah
D. Jumlah molekul gas berkurang maka energi kinetik molekul akan bertambah
E. Volume gas bertambah maka jumlah molekul gas bertambah
Pembahasan
Ruangan tertutup sehingga walaupun tekanan gas berubah, volume gas dalam tabung tidak berubah.
Jawaban yang benar adalah C.
2. Soal UN 2007/2008
Tekanan gas ideal di dalam ruang tertutup terhadap dinding tabung dirumuskan sebagai P = (2N / 3V) EK. P = tekanan (Pa), N = jumlah molekul (partikel) gas dan EK adalah energi kinetik rata-rata molekul (J). Berdasarkan persamaan ini, pernyataan yang benar adalah …
A. Tekanan gas terhadap dinding bergantung pada energi kinetik rata-rata molekul
B. Energi kinetik gas bergantung pada tekanan yang ditimbulkan molekul terhadap dinding
C. Suhu gas dalam tabung akan berubah jika tekanan gas berubah
D. Jika jumlah molekul gas berkurang maka volume energi kinetik molekul akan berkurang
E. Jika volume gas bertambah maka tekanan gas akan berkurang
Pembahasan
Diketahui :
Rumus tekanan : P = (2N / 3V) EK
P = tekanan
N = jumlah molekul partikel gas
V = volume gas
EK = energi kinetik rata-rata
P berbanding lurus dengan N dan EK
P berbanding terbalik dengan V
N berbanding lurus dengan volume
N berbanding terbalik dengan EK
Ditanya : Pernyataan yang benar
Jawab :
A salah karena berdasarkan rumus di atas, tekanan gas (P) bergantung pada energi kinetik, bukan energi kinetik rata-rata.
B salah karena tekanan bergantung pada energi kinetik gas, bukan sebaliknya.
C salah karena berdasarkan rumus di atas, suhu tidak bergantung pada tekanan
D salah karena N berbanding terbalik dengan EK, artinya jika N besar maka EK besar.
E benar karena tekanan (P) berbanding terbalik dengan volume (V).
Jawaban yang benar adalah E.
3. Soal UN 2008/2009 P04 No.16
Gas ideal yang berada dalam suatu bejana dimampatkan (ditekan), maka gas akan mengalami….
A. Penurunan laju partikel
B. Penurunan suhu
C. Kenaikan suhu
D. Penambahan partikel gas
E. Penurunan partikel gas
Pembahasan
Hukum gas ideal (dalam jumlah mol) :
PV = nRT
Hukum gas ideal (dalam jumlah molekul) :
PV = NkT
Hubungan antara energi kinetik dan suhu gas :
EK = 3/2 kT
Keterangan :
P = tekanan, V = volume, T = suhu, n = jumlah mol, N = jumlah molekul, R = konstanta umum gas, k = konstanta Boltzmann
Berdasarkan tiga rumus di atas, disimpulkan sebagai berikut :
– Jika gas ditekan maka volume (V) gas berkurang.
– Jika volume (V) gas berkurang maka tekanan (P) gas bertambah dan suhu (T) gas bertambah.
– Ruangan tertutup (V konstan) karenanya jumlah mol gas (n) dan jumlah partikel gas (N) tidak berubah.
– Jika suhu (T) gas bertambah maka energi kinetik (EK) gas bertambah. Jika energi kinetik gas bertambah maka kecepatan gerak partikel gas bertambah (EK = ½ m v2, v = kelajuan).
Jawaban yang benar adalah C.
4. Soal UN 2008/2009 P04 No.17
Sejumlah gas ideal dalam tabung tertutup dipanaskan secara isokhorik sehingga suhunya naik menjadi empat kali suhu semula. Energi kinetik rata-rata molekul gas ideal menjadi….
A. ¼ kali semula
B. ½ kali semula
C. Sama dengan semula
D. 2 kali semula
E. 4 kali semula
Pembahasan
Isokhorik = volume konstan
Hubungan antara energi kinetik rata-rata (EK) dan suhu (T) gas dinyatakan melalui persamaan di bawah :
EK = 3/2 kT
Keterangan : EK = energi kinetik, T = suhu, 3/2 = konstanta, k = konstanta Boltzmann.
Berdasarkan rumus ini tampak bahwa energi kinetik berbanding lurus dengan suhu. Jadi semakin besar suhu, semakin besar energi kinetik. Jika suhu naik menjadi empat kali semula maka energi kinetik juga naik menjadi empat kali semula.
Jawaban yang benar adalah E.
5. Soal UN 2008/2009 P45 No.14
Suatu gas ideal dengan tekanan P dan volume V dalam ruang tertutup. Jika tekanan gas dalam ruang tersebut diturunkan menjadi 1/4 kali semula pada volume tetap, maka perbandingan energi kinetik sebelum dan sesudah penurunan tekanan adalah…
A. 1 : 4
B. 1 : 2
C. 2 : 1
D. 4 : 1
E. 5 : 1
Pembahasan
Diketahui :
Volume awal = V
Volume akhir = V
Tekanan awal gas = P
Tekanan akhir gas = ¼ P
Ditanya : perbandingan energi kinetik awal dan energi kinetik akhir (EK1 : EK2)
Jawab :
Hubungan antara tekanan (P), volume (V) dan energi kinetik (EK) gas :

Perbandingan energi kinetik awal dan energi kinetik akhir :

Jawaban yang benar adalah D.
6. Soal UN 2009/2010 P70 No.16
Suhu gas ideal dalam tabung dirumuskan sebagai EK = 3/2 kT, T menyatakan suhu mutlak dan EK = energi kinetik rata-rata molekul gas. Beradasarkan persamaan di atas…
A. Semakin tinggi suhu gas, energi kinetiknya semakin kecil
B. Semakin tinggi suhu gas, gerak partikel gas semakin lambat
C. Semakin tinggi suhu gas, gerak partikel gas semakin cepat
D. Suhu gas berbanding terbalik dengan energi kinetik gas
E. Suhu gas tidak mempengaruhi gerak partikel gas
Pembahasan
Berdasarkan rumus di atas, suhu berbanding lurus dengan energi kinetik. Semakin tinggi suhu, semakin besar energi kinetik. Energi kinetik sebanding dengan kecepatan gerak partikel gas (EK = ½ m v2, di mana EK = energi kinetik, v = kecepatan). Semakin besar energi kinetik, semakin cepat gerakan partikel gas.
Jawaban yang benar adalah C.
7. Soal UN 2010/2011 P12 No.4
Faktor yang mempengaruhi energi kinetik gas di dalam ruang tertutup :
(1) tekanan
(2) volume
(3) suhu
(4) jenis zat
Pernyataan yang benar adalah….
A. (1) dan (2)
B. (1) dan (3)
C. (1) dan (4)
D. (2) saja
E. (3) saja
Pembahasan
Ruang tertutup karenanya volume gas konstan, volume gas tidak mempengaruhi energi kinetik.
Jawaban yang benar adalah B.
Teori kinetik gas 91.15 KB
Pembahasan soal termodinamika
Proses Termodinamika
1. Soal UN Fisika SMA 2012/2013 SA 55 No.18
Pada termodinamika, gas ideal mengalami proses isotermik jika…
A. perubahan keadaan gas suhunya selalu tetap
B. semua molekul bergerak dengan kecepatan berbeda
C. semua keadaan gas suhunya selalu berubah
D. pada suhu tinggi kecepatan molekulnya lebih tinggi
E. tekanan dan volume gas tidak mengalami perubahan
Pembahasan
Isotermal atau isotermik artinya suhu tetap.
Jawaban yang benar adalah A.
2. Soal UN Fisika SMA 2012/2013 SA 60 No.18
Semua gas ideal mengalami proses isokhorik sehingga…
A. semua molekul kecepatannya sama
B. pada suhu tinggi kecepatan rata-rata molekul lebih besar
C. tekanan gas menjadi tetap
D. gas akan melakukan usaha
E. tidak memiliki energi dalam
Pembahasan
Isokhorik = volume tetap.
Jawaban yang benar adalah B.
3. Soal UN Fisika SMA 2012/2013 SA 67 No.18
Pernyataan yang benar tentang proses termodinamika adalah…
A. isobarik adalah proses perubahan gas pada tekanan tetap
B. isobarik adalah proses perubahan gas pada suhu tetap
C. isokhorik merupakan proses perubahan gas pada tekanan tetap
D. isotermis adalah proses perubahan gas pada volume tetap
E. isokhorik adalah proses perubahan gas pada suhu tetap
Pembahasan
Isobarik = tekanan tetap
Isokhorik = volume tetap
Isotermis = suhu tetap
Jawaban yang benar adalah A.
Hukum I Termodinamika
4. Soal UN 1999/2000 No. 36
Dari grafik P-V di bawah, besar usaha gas pada proses I dan II berbanding sebagai …
A. 4 : 3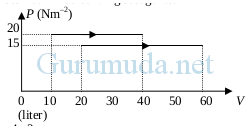
B. 3 : 4
C. 2 : 3
D. 1 : 2
E. 1 : 1
Pembahasan
Diketahui :
Proses 1 :
Tekanan (P) = 20 N/m2
Volume awal (V1) = 10 liter = 10 dm3 = 10 x 10-3 m3
Volume akhir (V2) = 40 liter = 40 dm3 = 40 x 10-3 m3
Proses 2 :
Tekanan (P) = 15 N/m2
Volume awal (V1) = 20 liter = 20 dm3 = 20 x 10-3 m3
Volume akhir (V2) = 60 liter = 60 dm3 = 60 x 10-3 m3
Ditanya :
Jawab :
Usaha gas pada proses I :
W = P ΔV = P (V2–V1) = (20)(40-10)(10-3 m3) = (20)(30)(10-3 m3) = (600)(10-3 m3) = 0,6 m3
Usaha gas pada proses II :
W = P ΔV = P (V2–V1) = (15)(60-20)(10-3 m3) = (15)(40)(10-3 m3) = (600)(10-3 m3) = 0,6 m3
Perbandingan usaha gas pada proses I dan II :
0,6 m3 : 0,6 m3
1 : 1
Jawaban yang benar adalah E.
5. Soal UN 2002/2003
Dari grafik P – V, besar usaha gas pada proses I dan II berbanding sebagai …
A. 4 : 3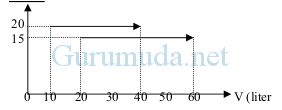
B. 3 : 4
C. 2 : 3
D. 1 : 2
E. 1 : 1
Pembahasan
Diketahui :
Proses I :
Tekanan (P) = 20 Pascal
Volume 1 (V1) = 10 liter
Volume 2 (V2) = 40 liter
Proses II :
Tekanan (P) = 15 Pascal
Volume 1 (V1) = 20 liter
Volume 2 (V2) = 60 liter
Ditanya : Perbandingan usaha gas pada proses I dan II
Jawab :
Proses termodinamika berdasarkan grafik di atas adalah proses isobarik (tekanan tetap).
Usaha yang dilakukan oleh gas pada proses I :
W = P (V2 – V1)
W = (20)(40 – 10)
W = (20)(30)
W = 600
Usaha yang dilakukan oleh gas pada proses II :
W = P (V2 – V1)
W = (15)(60 – 20)
W = (15)(40)
W = 600
Perbandingan usaha gas pada proses I dan II :
600 : 600
1 : 1
Jawaban yang benar adalah E.
6. Soal UN 2009/2010 P70 No.13
Gas helium dipanaskan sesuai grafik PV di bawah ini. Usaha yang dilakukan gas helium pada proses AB adalah…
A. 15 joule 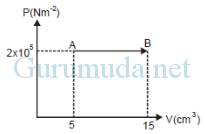
B. 10 joule
C. 8 joule
D. 4 joule
E. 2 joule
Pembahasan
Diketahui :
Tekanan (P) = 2 x 105 N/m2 = 2 x 105 Pascal
Volume awal (V1) = 5 cm3 = 5 x 10-6 m3
Volume akhir (V2) = 15 cm3 = 15 x 10-6 m3
Ditanya : Usaha yang dilakukan gas pada proses AB
Jawab :
W = ∆P ∆V
W = P (V2 – V1)
W = (2 x 105)(15 x 10-6 – 5 x 10-6)
W = (2 x 105)(10 x 10-6) = (2 x 105)(1 x 10-5)
W = 2 Joule
Jawaban yang benar adalah E.
7. Soal UN 2011/2012 C61 No.19
Perhatikan gambar! Gas ideal melakukan proses perubahan tekanan (P) terhadap volume (V). Usaha yang dilakukan oleh gas pada proses tersebut adalah…
A. 20 Joule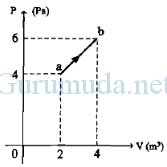
B. 15 Joule
C. 10 Joule
D. 5 Joule
E. 4 Joule
Pembahasan
Diketahui :
Tekanan awal (P1) = 4 Pa = 4 N/m2
Tekanan akhir (P2) = 6 Pa = 6 N/m2
Volume awal (V1) = 2 m3
Volume akhir (V2) = 4 m3
Ditanya : Usaha yang dilakukan oleh gas (W)
Jawab :
Usaha yang dilakukan gas = luasan di bawah kurva a-b.
W = luas segitiga + luas persegi panjang
W = ½ (6-4)(4-2) + 4(4-2)
W = ½ (2)(2) + 4(2)
W = 2 + 8
W = 10 Joule
Jawaban yang benar adalah E.
8. Soal UN 2011/2012 A81 No.19
Suatu gas ideal mengalami proses tertutup A → B → C → A. Dalam suatu siklus gas tersebut melakukan usaha sebesar….
A. −2,0 x 103 J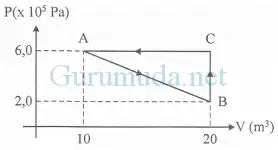
B. −5,5 x 103 J
C. −8,0 x 105 J
D. 2,0 x 106 J
E. 4,0 x 106 J
Pembahasan
Usaha (W) = luasan kurva (luasan segitiga di dalam garis bertanda panah).
W = ½ (20-10)(6 x 105 – 2 x 105)
W = ½ (10)(4 x 105)
W = (5)(4 x 105)
W = 20 x 105 = 2 x 106 Joule
Jawaban yang benar adalah D.
Mesin Kalor
9. Soal UN 2005/2006
Sebuah mesin menyerap panas sebesar 2.000 Joule dari suatu reservoir suhu tinggi dan membuangnya sebesar 1.200 Joule pada reservoir suhu rendah. Efisiensi mesin itu adalah ….
A. 80 %
B. 75 %
C. 60 %
D. 50 %
E. 40 %
Pembahasan
Diketahui :
Kalor yang diserap (QH) = 2000 Joule
Kalor yang dibuang (QL) = 1200 Joule
Usaha yang dihasilkan mesin (W) = 2000 – 1200 = 800 Joule
Ditanya : Efisiensi mesin kalor (e)
Jawab :
Rumus efisiensi mesin kalor :
e = W / QH = 800/2000 = 0,4 x 100% = 40%
Jawaban yang benar adalah E.
Mesin Carnot
10. Soal UN 2000/2001
Efisiensi mesin Carnot yang tiap siklusnya menyerap kalor pada suhu 960 K dan membuang kalor pada suhu 576 K adalah …
A. 40 %
B. 50 %
C. 56 %
D. 60 %
E. 80 %
Pembahasan
Diketahui :
Suhu tinggi (TH) = 960 K
Suhu rendah (TL) = 576 K
Ditanya : Efisiensi mesin Carnot (e)
Jawab :
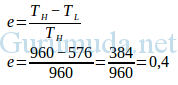
Efisiensi mesin Carnot adalah 0,4 x 100% = 40%
Jawaban yang benar adalah A.
11. Soal UN 2003/2004
Pada grafik PV mesin Carnot di bawah ini, W = 6.000 Joule. Banyak kalor yang dilepas oleh mesin tiap siklus adalah …
A. 2.250 joule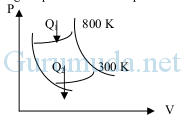
B. 3.000 joule
C. 3.750 joule
D. 6.000 joule
E. 9.600 joule
Pembahasan
Diketahui :
Usaha (W) = 6000 Joule
Suhu tinggi (TH) = 800 Kelvin
Suhu rendah (TL) = 300 Kelvin
Ditanya : Q
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
![]()
Kalor yang diserap oleh mesin Carnot :
W = e Q1
6000 = (0,625) Q1
Q1 = 6000 / 0,625
Q1 = 9600
Kalor yang dilepas oleh mesin Carnot :
Q2 = Q1 – W
Q2 = 9600 – 6000
Q2 = 3600 Joule
Tidak ada jawaban yang benar.
12. Soal UN 2006/2007
Sebuah mesin Carnot yang memiliki efisiensi 40% menggunakan reservoir panas yaag bersuhu 727°C. Tentukan suhu reservoir dingin!
A. 327°C
B. 357°C
C. 400°C
D. 600°C
E. 627°C
Pembahasan
Diketahui :
Efisiensi (e) = 40% = 40/100 = 0,4
Suhu tinggi (TH) = 727oC + 273 = 1000 K
Ditanya : Tentukan suhu reservoir dingin
Jawab :
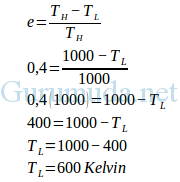
Suhu reservoir adalah 600–273 = 327oC
Jawaban yang benar adalah A.
13. Soal UN 2007/2008
Grafik P –V dari sebuah mesin Carnot terlihat seperti gambar berikut! Jika mesin menyerap kalor 800 J, maka usaha yang dilakukan adalah…
A. 105,5 J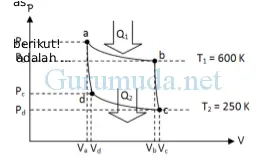
B. 252,6 J
C. 336,6 J
D. 466,7 J
E. 636,7 J
Pembahasan
Diketahui :
Suhu tinggi (TH) = 600 Kelvin
Suhu rendah (TL) = 250 Kelvin
Kalor yang diserap (Q1) = 800 Joule
Ditanya : Usaha (W)
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
![]()
Usaha yang dilakukan adalah :
W = e Q1
W = (7/12)(800 Joule)
W = 466,7 Joule
Jawaban yang benar adalah D.
14. Soal UN 2008/2009 P04 No.18
Mesin Carnot bekerja pada suhu tinggi 600 K, untuk menghasilkan kerja mekanik. Jika mesin menyerap kalor 600 J dengan suhu rendah 400 K maka usaha yang dihasilkan adalah….
A. 120 J
B. 124 J
C. 135 J
D. 148 J
E. 200 J
Pembahasan
Diketahui :
Suhu rendah (TL) = 400 K
Suhu tinggi (TH) = 600 K
Kalor yang diserap (Q1) = 600 Joule
Ditanya : Usaha yang dihasilkan mesin Carnot (W)
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
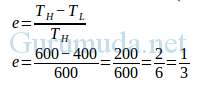
Usaha yang dilakukan oleh mesin Carnot :
W = e Q1
W = (1/3)(600) = 200 Joule
Jawaban yang benar adalah E.
Termodinamika 188.28 KB
Pembahasan soal termodinamika
Proses Termodinamika
1. Soal UN Fisika SMA 2012/2013 SA 55 No.18
Pada termodinamika, gas ideal mengalami proses isotermik jika…
A. perubahan keadaan gas suhunya selalu tetap
B. semua molekul bergerak dengan kecepatan berbeda
C. semua keadaan gas suhunya selalu berubah
D. pada suhu tinggi kecepatan molekulnya lebih tinggi
E. tekanan dan volume gas tidak mengalami perubahan
Pembahasan
Isotermal atau isotermik artinya suhu tetap.
Jawaban yang benar adalah A.
2. Soal UN Fisika SMA 2012/2013 SA 60 No.18
Semua gas ideal mengalami proses isokhorik sehingga…
A. semua molekul kecepatannya sama
B. pada suhu tinggi kecepatan rata-rata molekul lebih besar
C. tekanan gas menjadi tetap
D. gas akan melakukan usaha
E. tidak memiliki energi dalam
Pembahasan
Isokhorik = volume tetap.
Jawaban yang benar adalah B.
3. Soal UN Fisika SMA 2012/2013 SA 67 No.18
Pernyataan yang benar tentang proses termodinamika adalah…
A. isobarik adalah proses perubahan gas pada tekanan tetap
B. isobarik adalah proses perubahan gas pada suhu tetap
C. isokhorik merupakan proses perubahan gas pada tekanan tetap
D. isotermis adalah proses perubahan gas pada volume tetap
E. isokhorik adalah proses perubahan gas pada suhu tetap
Pembahasan
Isobarik = tekanan tetap
Isokhorik = volume tetap
Isotermis = suhu tetap
Jawaban yang benar adalah A.
Hukum I Termodinamika
4. Soal UN 1999/2000 No. 36
Dari grafik P-V di bawah, besar usaha gas pada proses I dan II berbanding sebagai …
A. 4 : 3
B. 3 : 4
C. 2 : 3
D. 1 : 2
E. 1 : 1
Pembahasan
Diketahui :
Proses 1 :
Tekanan (P) = 20 N/m2
Volume awal (V1) = 10 liter = 10 dm3 = 10 x 10-3 m3
Volume akhir (V2) = 40 liter = 40 dm3 = 40 x 10-3 m3
Proses 2 :
Tekanan (P) = 15 N/m2
Volume awal (V1) = 20 liter = 20 dm3 = 20 x 10-3 m3
Volume akhir (V2) = 60 liter = 60 dm3 = 60 x 10-3 m3
Ditanya :
Jawab :
Usaha gas pada proses I :
W = P ΔV = P (V2–V1) = (20)(40-10)(10-3 m3) = (20)(30)(10-3 m3) = (600)(10-3 m3) = 0,6 m3
Usaha gas pada proses II :
W = P ΔV = P (V2–V1) = (15)(60-20)(10-3 m3) = (15)(40)(10-3 m3) = (600)(10-3 m3) = 0,6 m3
Perbandingan usaha gas pada proses I dan II :
0,6 m3 : 0,6 m3
1 : 1
Jawaban yang benar adalah E.
5. Soal UN 2002/2003
Dari grafik P – V, besar usaha gas pada proses I dan II berbanding sebagai …
A. 4 : 3
B. 3 : 4
C. 2 : 3
D. 1 : 2
E. 1 : 1
Pembahasan
Diketahui :
Proses I :
Tekanan (P) = 20 Pascal
Volume 1 (V1) = 10 liter
Volume 2 (V2) = 40 liter
Proses II :
Tekanan (P) = 15 Pascal
Volume 1 (V1) = 20 liter
Volume 2 (V2) = 60 liter
Ditanya : Perbandingan usaha gas pada proses I dan II
Jawab :
Proses termodinamika berdasarkan grafik di atas adalah proses isobarik (tekanan tetap).
Usaha yang dilakukan oleh gas pada proses I :
W = P (V2 – V1)
W = (20)(40 – 10)
W = (20)(30)
W = 600
Usaha yang dilakukan oleh gas pada proses II :
W = P (V2 – V1)
W = (15)(60 – 20)
W = (15)(40)
W = 600
Perbandingan usaha gas pada proses I dan II :
600 : 600
1 : 1
Jawaban yang benar adalah E.
6. Soal UN 2009/2010 P70 No.13
Gas helium dipanaskan sesuai grafik PV di bawah ini. Usaha yang dilakukan gas helium pada proses AB adalah…
A. 15 joule 
B. 10 joule
C. 8 joule
D. 4 joule
E. 2 joule
Pembahasan
Diketahui :
Tekanan (P) = 2 x 105 N/m2 = 2 x 105 Pascal
Volume awal (V1) = 5 cm3 = 5 x 10-6 m3
Volume akhir (V2) = 15 cm3 = 15 x 10-6 m3
Ditanya : Usaha yang dilakukan gas pada proses AB
Jawab :
W = ∆P ∆V
W = P (V2 – V1)
W = (2 x 105)(15 x 10-6 – 5 x 10-6)
W = (2 x 105)(10 x 10-6) = (2 x 105)(1 x 10-5)
W = 2 Joule
Jawaban yang benar adalah E.
7. Soal UN 2011/2012 C61 No.19
Perhatikan gambar! Gas ideal melakukan proses perubahan tekanan (P) terhadap volume (V). Usaha yang dilakukan oleh gas pada proses tersebut adalah…
A. 20 Joule
B. 15 Joule
C. 10 Joule
D. 5 Joule
E. 4 Joule
Pembahasan
Diketahui :
Tekanan awal (P1) = 4 Pa = 4 N/m2
Tekanan akhir (P2) = 6 Pa = 6 N/m2
Volume awal (V1) = 2 m3
Volume akhir (V2) = 4 m3
Ditanya : Usaha yang dilakukan oleh gas (W)
Jawab :
Usaha yang dilakukan gas = luasan di bawah kurva a-b.
W = luas segitiga + luas persegi panjang
W = ½ (6-4)(4-2) + 4(4-2)
W = ½ (2)(2) + 4(2)
W = 2 + 8
W = 10 Joule
Jawaban yang benar adalah E.
8. Soal UN 2011/2012 A81 No.19
Suatu gas ideal mengalami proses tertutup A → B → C → A. Dalam suatu siklus gas tersebut melakukan usaha sebesar….
A. −2,0 x 103 J
B. −5,5 x 103 J
C. −8,0 x 105 J
D. 2,0 x 106 J
E. 4,0 x 106 J
Pembahasan
Usaha (W) = luasan kurva (luasan segitiga di dalam garis bertanda panah).
W = ½ (20-10)(6 x 105 – 2 x 105)
W = ½ (10)(4 x 105)
W = (5)(4 x 105)
W = 20 x 105 = 2 x 106 Joule
Jawaban yang benar adalah D.
Mesin Kalor
9. Soal UN 2005/2006
Sebuah mesin menyerap panas sebesar 2.000 Joule dari suatu reservoir suhu tinggi dan membuangnya sebesar 1.200 Joule pada reservoir suhu rendah. Efisiensi mesin itu adalah ….
A. 80 %
B. 75 %
C. 60 %
D. 50 %
E. 40 %
Pembahasan
Diketahui :
Kalor yang diserap (QH) = 2000 Joule
Kalor yang dibuang (QL) = 1200 Joule
Usaha yang dihasilkan mesin (W) = 2000 – 1200 = 800 Joule
Ditanya : Efisiensi mesin kalor (e)
Jawab :
Rumus efisiensi mesin kalor :
e = W / QH = 800/2000 = 0,4 x 100% = 40%
Jawaban yang benar adalah E.
Mesin Carnot
10. Soal UN 2000/2001
Efisiensi mesin Carnot yang tiap siklusnya menyerap kalor pada suhu 960 K dan membuang kalor pada suhu 576 K adalah …
A. 40 %
B. 50 %
C. 56 %
D. 60 %
E. 80 %
Pembahasan
Diketahui :
Suhu tinggi (TH) = 960 K
Suhu rendah (TL) = 576 K
Ditanya : Efisiensi mesin Carnot (e)
Jawab :
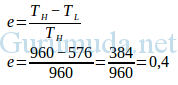
Efisiensi mesin Carnot adalah 0,4 x 100% = 40%
Jawaban yang benar adalah A.
11. Soal UN 2003/2004
Pada grafik PV mesin Carnot di bawah ini, W = 6.000 Joule. Banyak kalor yang dilepas oleh mesin tiap siklus adalah …
A. 2.250 joule
B. 3.000 joule
C. 3.750 joule
D. 6.000 joule
E. 9.600 joule
Pembahasan
Diketahui :
Usaha (W) = 6000 Joule
Suhu tinggi (TH) = 800 Kelvin
Suhu rendah (TL) = 300 Kelvin
Ditanya : Q
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
![]()
Kalor yang diserap oleh mesin Carnot :
W = e Q1
6000 = (0,625) Q1
Q1 = 6000 / 0,625
Q1 = 9600
Kalor yang dilepas oleh mesin Carnot :
Q2 = Q1 – W
Q2 = 9600 – 6000
Q2 = 3600 Joule
Tidak ada jawaban yang benar.
12. Soal UN 2006/2007
Sebuah mesin Carnot yang memiliki efisiensi 40% menggunakan reservoir panas yaag bersuhu 727°C. Tentukan suhu reservoir dingin!
A. 327°C
B. 357°C
C. 400°C
D. 600°C
E. 627°C
Pembahasan
Diketahui :
Efisiensi (e) = 40% = 40/100 = 0,4
Suhu tinggi (TH) = 727oC + 273 = 1000 K
Ditanya : Tentukan suhu reservoir dingin
Jawab :
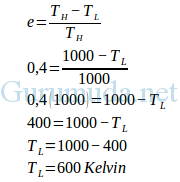
Suhu reservoir adalah 600–273 = 327oC
Jawaban yang benar adalah A.
13. Soal UN 2007/2008
Grafik P –V dari sebuah mesin Carnot terlihat seperti gambar berikut! Jika mesin menyerap kalor 800 J, maka usaha yang dilakukan adalah…
A. 105,5 J
B. 252,6 J
C. 336,6 J
D. 466,7 J
E. 636,7 J
Pembahasan
Diketahui :
Suhu tinggi (TH) = 600 Kelvin
Suhu rendah (TL) = 250 Kelvin
Kalor yang diserap (Q1) = 800 Joule
Ditanya : Usaha (W)
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
![]()
Usaha yang dilakukan adalah :
W = e Q1
W = (7/12)(800 Joule)
W = 466,7 Joule
Jawaban yang benar adalah D.
14. Soal UN 2008/2009 P04 No.18
Mesin Carnot bekerja pada suhu tinggi 600 K, untuk menghasilkan kerja mekanik. Jika mesin menyerap kalor 600 J dengan suhu rendah 400 K maka usaha yang dihasilkan adalah….
A. 120 J
B. 124 J
C. 135 J
D. 148 J
E. 200 J
Pembahasan
Diketahui :
Suhu rendah (TL) = 400 K
Suhu tinggi (TH) = 600 K
Kalor yang diserap (Q1) = 600 Joule
Ditanya : Usaha yang dihasilkan mesin Carnot (W)
Jawab :
Efisiensi mesin kalor ideal (mesin Carnot) :
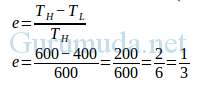
Usaha yang dilakukan oleh mesin Carnot :
W = e Q1
W = (1/3)(600) = 200 Joule
Jawaban yang benar adalah E.
Termodinamika 188.28 KB

0 Response to "√Pembahasan Soal Teori Kinetik Gas ⊗ Full Pembahasanya"
Posting Komentar